Окислительно восстановительные реакции в свинцово кислотном аккумуляторе. Электрохимические элементы. Примерные вопросы для самооценки
При помещении металлического цинка в раствор сульфата меди происходит окислительно-восстановительная реакция:
Zn (т) + Cu 2+ → Zn 2+ + Cu (т)
Обе полуреакции (восстановления и окисления) происходят одновременно в месте соприкосновения цинка с раствором. Цинк отдает два электрона катиону меди, окисляясь при этом.
Если же поступить наоборот и поместить металлическую медь в раствор сульфата цинка, то ничего не произойдет. Помните об активности металлов! Цинк является более активным, чем медь - он легче отдает электроны.
В рассмотренном выше примере обе полуреакции протекали в одном месте. А что будет, если разделить полуреакции восстановления и окисления? В этом случае электроны будут переходить от восстановителя к окислителю по внешней цепи, которая будет служить проводником электрического тока. Да-да - направленный поток электронов есть не что иное, как электрический ток.
Устройство преобразования энергии химических реакций в электроэнергию, называются гальваническими элементами , или, говоря простым языком, - электрическими батарейками.
Медная пластинка (отрицательный электрод - анод) погружена в емкость с сульфатом меди.
Цинковая пластинка (положительный электрод - катод) - в раствор сульфата цинка.
Пластинки соединены между собой металлическим проводником. Но для того, чтобы в цепи появился электрический ток, необходимо соединить емкости соляным мостом (трубка, заполненная концентрированной соляным раствором). Соляной мост позволяет ионам перемещаться из одной емкости в другую, при этом растворы остаются электрически нейтральными. Что происходит с системой?
Цинк окисляется: атомы цинка превращаются в ионы и переходят в раствор. Высвободившиеся электроны движутся по внешней цепи к медному электроду, где происходит восстановление ионов меди. Приходящие сюда электроны соединяются с выходящими из раствора ионами меди. При этом образуются атомы меди, выделяющиеся в виде металла. Катионы соляного моста перемещаются в емкость с медным электродом для замещения расходуемых ионов меди. Анионы соляного моста перемещаются в емкость с цинковым электродом, помогая сохранять электрически нейтральный раствор с образующимися катионами цинка.
Разность потенциалов (напряжение) в такой системе будет тем больше, чем дальше металлы находятся друг от друга в ряду активности.
2. Сухой элемент
В бытовых электрических батарейках используется сухой элемент, состоящий из:
- цинкового корпуса (анод);
- находящегося внутри корпуса графитового стержня (катод).
Стержень окружен слоем оксида марганца и угольной сажи, в качестве электролита используется слой хлорида аммония и хлорида цинка. В результате этого происходят следующие реакции:
- реакция окисления: Zn (т) → Zn 2+ + e -
- реакция восстановления: 2MnO 2 (т) + 2NH 4 + + 2e - → Mn 2 O 3 (т) + 2NH 3 (р-р) + H 2 O (ж)
В щелочном сухом элементе вместо кислой среды хлорида аммония в качестве электролита используется щелочная среда гидроксида калия, что повышает срок службы элемента, т.к., корпус не так быстро корродирует.
Основным недостатком гальванических элементов является тот факт, что производство электричества идет до тех пор, пока не закончится один из реагентов.
3. Аккумуляторы
Аккумуляторы устраняют главный недостаток сухих элементов - короткий срок службы, поскольку могут перезаряжаться, а потому, время их эксплуатации повышается во много раз и составляет несколько лет.
Обычный свинцовый аккумулятор состоит из шести, последовательно соединенных, элементов (банок). Каждая банка дает напряжение 2В, а их сумма = 12В.
В качестве анода используется свинец. Катод - диоксид свинца (PbO 2). Электроды погружены в раствор серной кислоты (H 2 SO 4). При замыкании цепи в аккумуляторе происходят следующие реакции:
На аноде: Pb (т) + H 2 SO 4 (p-p) → PbSO 4 (т) + 2H + + 2e -
На катоде: 2e - +2H + + PbO2 (т) + H 2 SO 4 (p-p) → PbSO 4 (т) + 2H 2 O (ж)
Общая: Pb (т) + PbO 2 (т) + 2H 2 SO 4 (p-p) → 2PbSO 4 (т) + 2H 2 O (ж)
Аккумулятор (при исправном состоянии автомобиля) служит только для пуска двигателя. В момент пуска в цепи протекает довольно значительный ток (десятки ампер), поэтому, заряд аккумулятора расходуется очень быстро (за несколько минут). После того, как двигатель запущен, всё электропитание автомобиля берет на себя генератор. Во время работы двигателя генератор подзаряжает аккумулятор: первоначальные окислительно-восстановительные реакции протекают в обратном направлении:
2PbSO 4 (т) + 2H 2 O (ж) → Pb (т) + PbO 2 (т) + 2H 2 SO 4 (p-p)
В результате восстанавливается свинец и диоксид свинца.
4. Гальваническое покрытие
Суть электролитических элементов состоит в осуществлении за счет электроэнергии химических реакций - восстановления на катоде и окисления на аноде.
Окислительно-восстановительная реакция, протекающая на электродах при прохождении электротока через электролитический элемент, называется электролизом:
Электролиз воды: 2H 2 O (ж) → 2H 2 (г) + O 2 (г)
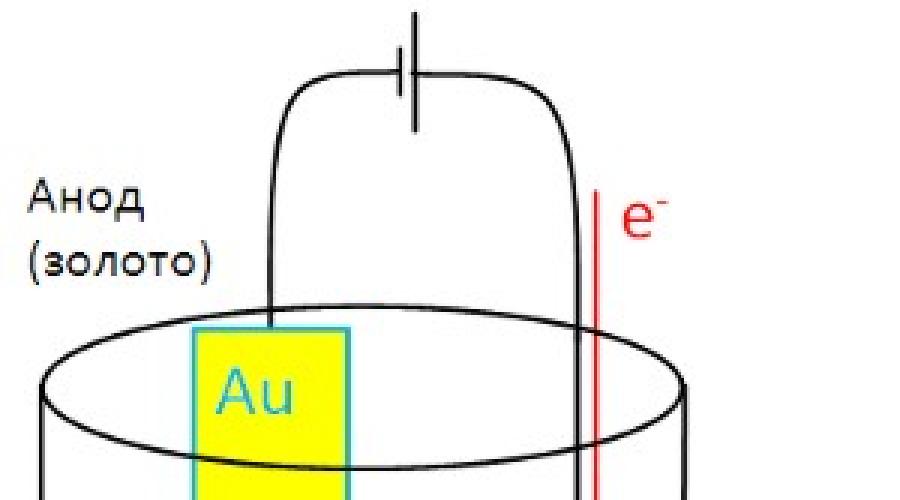
Электролитические элементы используются для получения гальванопокрытий . При этом один металл наносится тончайшим слоем на поверхность другого металла.

Источником электроэнергии при гальванопокрытии служит внешний источник тока. Брусок золота является источником ионов золота, которые восстанавливаются на поверхности медали.
Покрытия, нанесенные методом электролиза, получаются ровными по толщине и прочными. В итоге изделие внешне ничем не отличается от "чистого" варианта, а по цене - существенно дешевле.
Электрохимия
Зайлобов Л. Т., аспирант Ташкентского государственного педагогического университета им. Низами (Узбекистан)
ДЕМОНСТРАЦИЯ ПРОЦЕССОВ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ РЕАКЦИЙ, ПРОХОДЯЩИХ В СВИНЦОВОМ АККУМУЛЯТОРЕ, С ПРИМЕНЕНИЕМ ИННОВАЦИОННЫХ ТЕХНОЛОГИЙ
Представлена анимационная модель демонстрации процессов окислительно-восстановительных реакций, проходящих в свинцовом аккумуляторе, с применением инновационных технологий. Данная статья рекомендована для учащихся академических лицеев и колледжей с углубленным изучением химии.
Ключевые слова: окислительно-восстановительные реакции, гальванические элемент, батарея, свинцовом аккумуляторе, растворе H2S04, электрод, анимационная модель, металлического свинца, исход электрического тока - разряд, восстановление - заряд, ионы, электропроводность.
DEVELOPMENT OF EDUCATION ON OXIDATION-REDUCTION REACTIONS OCCURRING IN LEAD CELLS USING INNOVATIVE TECHNOLOGIES
Is presented animation model the development of the tuition of oxidizing-reсonstruсtion reactions passing in plumbum battery with applying of innovation technologies. This article is recommended for taken into account academic lyceums and colleges with the in-depth studies of chemistry.
Keywords: oxidizing-reconstruction reactions, galvanic element, a batterie, leaden battery, solution H2S04, electrode, animation model, metallic lead, upshot of the electric current - a category, reconstruction - a charge, Ions, conduction.
В настоящее время широко используемые гальванические элементы - батареи и аккумуляторы являются неотъемлемой частью нашей жизни. Окислительные и восстановительные процессы, которые проходят в аккумуляторах, являются одной из трудноосваиваемых тем общей химии. Объяснение данной темы без наглядных пособий и химических опытов является основной причиной этой проблемы.
Периодические перемещения электронов в окислительных и восстановительных реакциях, проходящие в гальванических элементах, можно показать только при помощи инновационных технологий. Динамичная модель этих процессов демонстрируется с помощью компьютера. Готовые электронные данные и проведение компьютерных уроков на основе анимации и их демонстрация ученикам повышают качество урока.
Свинцовая аккумуляторная батарея. В элементах протекают следующие реакции: На эноде: Pb+SO43^PbSO4+24
На катоде: Pb O2+ SO42+24^ PbSO4+2H2O Батарея обладает свойством обратимости (может перезаряжаться), поскольку продукт протекающих с ней реакций - образующийся на обоих электродах сульфат свинца - оседает на пластинах, а не диффундирует и не отваливается от них. Один элемент изображенный здесь свинцовой аккумуляторной батареи дает напряжение около 2 В; в батареях на 6 или 12 В последовательно соединены три или шесть описанных элементов.
Первый работоспособный свинцово-кислотный аккумулятор был изобретен в 1859 г. французским ученым Гастоном Планте. Конструкция аккумулятора представляла собой электроды из листового свинца, разделенные сепараторами из полотна, которые были свернуты в спираль и помещены в сосуд с 10 % раствором серной кислоты. Недостатком первых свинцово-кислотных аккумуляторов была их невысокая емкость.
В качестве примера рассмотрим готовый к употреблению свинцовый аккумулятор. Он состоит из решетчатых свинцовых пластин, одни из которых заполнены диоксидом свинца, а другие - металлическим губчатым свинцом. Пластины погружены в 35-40% раствор Н2804; при этой концентрации удельная электропроводность раствора серной кислоты максимальна.
При работе аккумулятора - при его разряде - в нем протекает окислительно-восстановительная реакция, в ходе которой металлический свинец окисляется:
РЬ+804-2=РЬ804+2ё или РЬ-2ё=РЬ+2
А диоксид свинца восстанавливается:
РЬ02+2Н2804=РЬ(804)2+2Н20
РЬ(804)2+2ё= РЬ804+ 80^2 или РЬ+4+2ё=РЬ
Электроны, отдаваемые атомами металлического свинца при окислении, принимаются атомами свинца РЬ02 при восстановлении; электроны передаются от одного электрода к другому по внешней цепи.
Таким образом, были созданы и испытаны химические процессы, проходящие в аккумуляторах в виде анимационной модели. В ней показан исход электрического тока - разряд и восстановление - заряд. Появление каждой реакции объясняется движением ионов в растворе.
р-1,23-1,27 гр/мл
Во внутренней цепи (в растворе Н2804) при работе аккумулятора происходит перенос
ионов. Ионы 804 движутся к аноду, а ионы Н+ - к катоду. Направление этого движения обусловлено электрическим полем, возникающим в результате протекания электродных процессов: у анода расходуются анионы, а у катода - катионы. В итоге раствор остается электронейтральным.
Если сложить уравнения, отвечающие окислению свинца и восстановлению РЬ02, то получится суммарное уравнение реакции, протекающей в свинцовом аккумуляторе при его работе (разряде):
РЬ + РЬ02 + 4Н++ 2Б04
2РЬБ04 + 2Н2О
Э.д.с. заряженного свинцового аккумулятора равна приблизительно 2В. По мере разряда аккумулятора материалы его катода (РЬ02) и анода (РЬ) расходуются. Расходуется и серная кислота. При этом напряжение на зажимах аккумулятора падает. Когда оно становится меньше значения, допускаемого условиями эксплуатации, аккумулятор вновь заряжают.
Для зарядки (или заряда) аккумулятор подключают к внешнему источнику тока (плюсом к плюсу и минусом к минусу). При этом ток протекает через аккумулятор в направлении, обратном тому, в котором он проходил при разряде аккумулятора. В результате этого электрохимические процессы на электродах «обращаются». На свинцовом электроде теперь происходит процесс восстановления:
РЬ804+2Н++2ё = Н2Б04 + РЬ т.е. данный электрод становится катодом. На электроде из РЬ02 идет процесс окисления:
РЬ804+2Н+-2ё=РЬ02+Н2804+2Н+
Следовательно, этот электрод является теперь анодом. Ионы в растворе движутся в направлениях, обратных тем, в которых они перемещались при работе аккумулятора.
Складывая два последних уравнения, получим уравнение реакции, протекающей при зарядке аккумулятора:
2РЬБ04 + 2Ш0^РЬ + РЬ02 + 2Н2Б04
Нетрудно заметить, что этот процесс противоположен тому, который протекает при работе аккумулятора: при зарядке аккумулятора в нем вновь получаются вещества, необходимые для его работы.
Свинцовые аккумуляторы являются наиболее распространенными среди всех существующих в настоящее время химических источников тока. Их масштабное производство определяется как относительно низкой ценой, обусловленной сравнительной недефицитностью исходных материалов, так и разработкой разных вариантов этих аккумуляторов, отвечающих требованиям широкого круга потребителей.
Применение наглядной демонстрации процессов, проходящих в данном свинцовом аккумуляторе, использование анимационной модели позволяет учащимся легче усвоить столь трудную для понимания тему.
ЛИТЕРАТУРА
1. Р.Дикерсон, Г.Грей, Дж.Хейт. Основные законы химии. Издательство «Мир» Москва 1982. 653с.
2. Деордиев С.С. Аккумуляторы и уход за ними. К.: Техника, 1985. 136с.
3. Электротехнический справочник. В 3-х т. Т.2. Электротехнические изделия и устройства/под общ. ред. профессоров МЭИ (гл. ред. И. Н. Орлов) и др. 7 изд. 6 испр. и доп. М.: Энергоатомиздат, 1986. 712 с.
Как не формулируй название статьи, - оно всё равно будет правильным. Химия и энергия - связаны воедино в конструкции аккумулятора.
Свинцово-кислотные аккумуляторы могут работать несколько лет в режимах заряда-разряда. Они быстро подзаряжаются и быстро отдают запасённую энергию. Секрет этих метаморфоз кроется в химии, ведь именно она помогает преобразовывать электричество, но как?
 «Таинство» преобразования энергии в аккумуляторе обеспечивает совокупность реагентов, среди которых есть окислитель и восстановитель, взаимодействующие через электролит. Восстановитель (губчатый свинец РЬ) имеет отрицательный заряд. Во время химической реакции он окисляется, и его электроны странствуют к окислителю, у которого положительный заряд. Окислитель (диоксид свинца РЬО2) восстанавливается, а результатом этого является электрический ток.
«Таинство» преобразования энергии в аккумуляторе обеспечивает совокупность реагентов, среди которых есть окислитель и восстановитель, взаимодействующие через электролит. Восстановитель (губчатый свинец РЬ) имеет отрицательный заряд. Во время химической реакции он окисляется, и его электроны странствуют к окислителю, у которого положительный заряд. Окислитель (диоксид свинца РЬО2) восстанавливается, а результатом этого является электрический ток.
В качестве электролита используют жидкость, которая плохо проводит ток, но является хорошим проводником для ионов. Это водный раствор серной кислоты (H2S04). В химической реакции происходит процесс, всем известный со школьной скамьи - электролитическая диссоциация.
В процессе реакции, - положительно заряженные ионы (Н+) направляются к положительному электроду, а отрицательно заряженные ионы (SO42-) к отрицательному. Когда аккумулятор разряжается, то из восстановителя (губчатый свинец), через электролит к положительному электроду, - направляются ионы с положительным зарядом РЬ2+.
Четырехвалентные ионы свинца (РЬ4+) превращаются в двухвалентные (РЬ4+). Однако, это еще не все химические реакции. Когда ионы кислотных остатков с отрицательным зарядом (SO42-) соединяются с положительно заряженными ионами свинца (РЬ2+), то на обоих электродах образуется сульфат свинца (РЬSО4). А вот это уже плохо для аккумулятора. Сульфатация сокращает срок службы аккумулятора и постепенно накапливаясь, может привести к его разрушению. Побочным эффектом химических реакций в обычных свинцово-кислотных аккумуляторах, являются газы.

Что же происходят, когда аккумулятор подзаряжают?
Электроны направляются к электроду с отрицательным зарядом, где выполняют свою функцию - нейтрализуют ионы свинца (РЬ2+). Химические реакции, происходящие в аккумуляторных батареях можно описать такой формулой:
Плотность электролита, и его уровень в аккумуляторе, зависит от того, - заряжен, или разряжен аккумулятор. Изменения плотности электролита можно описать следующей формулой:
![]()
Где показатель разрядки аккумулятора, который измеряется в процентах, - Cp. Плотность электролита при полной зарядке - Рз. Плотность электролита при полной разрядке - Pр.
Стандартная температура, при которой делают измерения + 25°С, Плотность электролита в соответствии с температурой + 25°С, г/см3 - Р25.
Во время химической реакции положительные электроды используют в 1,6 раза больше кислоты, чем отрицательные. Когда аккумулятор разряжается, то объем электролита растет, а когда заряжается, наоборот - уменьшается.
Таким вот образом, с помощью химических реакций, аккумулятор принимает, а потом отдаёт электрическую энергию.
Окислительно-восстановите льные реакции – реакции, которые идут с изменением степеней окисления элементов.
Окисление – процесс отдачи электронов.
Восстановление – процесс присоединения электронов.
Окислитель – атом, молекула или ион, который принимает электроны.
Восстановитель – атом, молекула или ион, который отдает электроны.
Окислители, принимая электроны, переходят в восстановленную форму:
F2 [ок. ] + 2ē → 2F¯ [восст.].
Восстановители, отдавая электроны, переходят в окисленную форму:
Na0 [восст. ] – 1ē → Na+ [ок.].
Равновесие между окисленной и восстановленной формами характеризуется с помощью уравнения Нернста для окислительно-восстановительного потенциала:
где Е0 – стандартное значение окислительно-восстановительного потенциала; n – число переданных электронов; [восст. ] и [ок. ] – молярные концентрации соединения в восстановленной и окисленной формах соответственно.
Величины стандартных электродных потенциалов Е0 приведены в таблицах и характеризуют окислительные и восстановительные свойства соединений: чем поло-жительнее величина Е0, тем сильнее окислительные свойства, и чем отрицательнее значение Е0, тем сильнее восстановительные свойства.
Например, для F2 + 2ē ↔ 2F¯Е0 = 2,87 вольт, а для Na+ + 1ē ↔ Na0Е0 = -2,71 вольт (процесс всегда записывается для реакций восстановления).
Окислительно-восстановительная реакция представляет собой совокупность двух полуреакций, окисления и восстановления, и характеризуется электродвижущей силой (э.д.с.) ΔЕ0: ΔЕ0 = ΔЕ0ок – ΔЕ0восст , где Е0ок и ΔЕ0восст – стандартные потенциалы окислителя и восстановителя для данной реакции.
Э.д.с. реакции ΔЕ0 связана с изменением свободной энергии Гиббса ΔG и константой равновесия реакции К:
ΔG = – nF ΔЕ0 или ΔЕ = (RT/nF) lnK.
Э.д.с. реакции при нестандартных концентрациях ΔЕ равна: ΔЕ = ΔЕ0 – (RT/nF) × IgK или ΔЕ = ΔЕ0 – (0,059/n )lgK .
В случае равновесия ΔG = 0 и ΔЕ = 0, откуда ΔЕ = (0,059/n)lgK и К = 10nΔE/0,059.
Для самопроизвольного протекания реакции должны выполняться соотношения: ΔG < 0 или К >> 1, которым соответствует условие ΔЕ0 > 0. Поэтому для определения возможности протекания данной окислительно-восстановительной реакции необходимо вычислить значение ΔЕ0. Если ΔЕ0 > 0, реакция идет. Если ΔЕ0 < 0, реакция не идет.
Химические источники тока
Гальванические элементы – устройства, преобразующие энергию химической реакции в электрическую энергию.
Гальванический элемент Даниэля состоит из цинкового и медного электродов, погруженных в растворы ZnSO4 и CuSO4 соответственно. Растворы электролитов сообщаются через пористую перегородку. При этом на цинковом электроде идет окисление: Zn → Zn2+ + 2ē, а на медном электроде – восстановление: Cu2+ + 2ē → Cu. В целом идет реакция: Zn + CuSO4 = ZnSO4 + Cu.
Анод – электрод, на котором идет окисление. Катод – электрод, на котором идет восстановление. В гальванических элементах анод заряжен отрицательно, а катод – положительно. На схемах элементов металл и раствор отделены вертикальной чертой, а два раствора – двойной вертикальной чертой.
Так, для реакции Zn + CuSO4 = ZnSO4 + Cu схемой гальванического элемента является запись: (-)Zn | ZnSO4 || CuSO4 | Cu(+).
Электродвижущая сила (э.д.с.) реакции равна ΔЕ0 = Е0ок – Е0восст = Е0 (Cu2+/Cu) – Е0 (Zn2+/Zn) = 0,34 – (-0,76) = 1,10 В. Из-за потерь напряжение, создаваемое элементом, будет несколько меньше, чем ΔЕ0. Если концентрации растворов отличаются от стандартных, равных 1 моль/л, то Е0ок и Е0восст вычисляются по уравнению Нернста, а затем вычисляется э.д.с. соответствующего гальванического элемента.
Сухой элемент состоит их цинкового корпуса, пасты NH4Cl с крахмалом или мукой, смеси MnO2 с графитом и графитового электрода. В ходе его работы идет реакция: Zn + 2NH4Cl + 2MnO2 = Cl + 2MnOOH.
Схема элемента: (-)Zn | NH4Cl | MnO2, C(+). Э.д.с. элемента – 1,5 В.
Свинцово–кислотный аккумулятор – на данный момент, этот тип аккумуляторов считается наиболее распространённым, нашел широкую область применения как автомобильный аккумулятор.
Принцип действия аккумулятора
Принцип действия, как говорилось ранее в статье про аккумуляторы , основан на окислительно-восстановительной электрохимической реакции. В данном случае на реакции свинца с диоксидом свинца, находящихся в сернокислотной среде. Во время использования аккумулятора, происходит разряд – на аноде будет происходить восстановление диоксида свинца, а на катоде – окисление свинца.
Во время зарядки аккумулятора, будут проходить ровно обратные реакции, с выделением кислорода на положительном электроде, и выделением водорода на отрицательном. Следует учесть, что на критических значениях, когда происходит зарядка и аккумулятор почти заряжен, может начать преобладать реакция электролиза воды, что приведет к её постепенному исчерпанию.
В итоге, можно сказать, что при заряде серная кислота будет выделяться в электролит, что влечет за собой повышение плотности электролита, а при разряде серная кислота будет расходоваться, и плотность будет падать.
Устройство аккумулятора
Свинцово-кислотный аккумулятор состоит из электродов, разделительных сепараторов (ячеек, изоляторов), которые находятся в электролите. Сами электроды на вид – это свинцовые решетки, только с разным активным веществом, положительный электрод имеет активное вещество – диоксид свинца (PbO 2), отрицательный электрод – свинец.

Рисунок 1 – Общий вид свинцово-кислотного аккумулятора

Рисунок 2 – Ячейка аккумулятора с положительными и отрицательными электродами, разделёнными сепараторами
На рисунке 1 вы можете видеть в моноблоке отдельные ячейки подробно рассмотренные на рисунке 2 – в которых находятся положительные и отрицательные электроды, разделённые сепараторами.
Эксплуатация свинцово-кислотного аккумулятора при низких температурах
В отличии от других типов аккумуляторов, свинцово-кислотные более-менее устойчивы к холоду, как мы видим в последствии – широкое применение на автотранспорте. Свинцово-кислотный аккумулятор теряет 1% своей ёмкости на каждый градус отличный от +20°C, что говорит о том, что при 0°C ёмкость свинцово-кислотного аккумулятора будет составлять лишь 80% его ёмкости. Это обусловлено увеличением вязкости электролита при низких температурах, из-за чего он не может поступать в нормальной степени к электродам, а тот электролит что поступает, быстро истощается.
Зарядка аккумулятора
Для большинства аккумуляторов ток зарядки должен быть написан на корпусе, примерно, он может находиться в пределах от 0.1 до 0.3 емкости аккумулятора. Вообще, общепринятым считается зарядка аккумулятора 10% током от его ёмкости, на протяжении 10 часов. Максимальное напряжение при зарядке не должно превышать 2.3 ± 0.023 В на каждый из элементов аккумулятора. То есть, можно сказать что для свинцового аккумулятора с напряжением в 12 В, напряжение во время зарядки не должно превышать 13.8 ± 0.15 В.
Хранение свинцово кислотных аккумуляторов
Свинцово-кислотные аккумуляторы хранятся только в заряженном состоянии. Хранение их в разряженном состоянии приводит к потере работоспособности.